随着免疫检查点抑制剂药物相关临床研究的不断探索,免疫治疗方案已被证明为晚期NSCLC患者带来了显著且长期的生存获益。随之而来,关于免疫检查点药物临床用药时长的讨论也成为目前临床上十分关注的话题之一。本篇综述文章就该热点话题进行了全方面的分析探讨,针对接受抗肿瘤免疫治疗且长期获益的NSCLC患者,希望在最大程度避免患者疾病进展或复发的前提下,减轻患者因用药所带来的药物毒性和经济负担。
【免疫用药时长与疗效关系的探索】
肺癌是发病率和死亡率最高的恶性肿瘤之一,其中非小细胞肺癌患者约占肺癌患者总人数的85%,而晚期NSCLC患者在初诊患者中占半数以上【1, 2】。得益于PD-1/PD-L1免疫检查点类药物的迅速发展,一线接受免疫检查点药物治疗的晚期NSCLC患者5年生存率已接近20%【3, 4】。基于在晚期NSCLC治疗中所展现出的显著疗效,无论PD-L1表达情况,NCCN指南已全面推荐晚期非鳞/鳞状NSCLC一线优先使用免疫检查点抑制剂类药物。截至目前,我国已批准多款PD-(L)1药物用于晚期NSCLC患者的一线治疗。除此之外,基于全球多中心III期RATIONALE-303研究,我国也已批准替雷利珠单抗用于治疗接受铂类化疗后出现疾病进展的二或三线局晚/晚期NSCLC患者【5】。
随着免疫治疗的广泛应用,临床实践中观察到了很多不同于传统治疗的非典型反应特征,为免疫治疗的临床决策带来了新的问题和挑战,例如在临床实践中,免疫治疗什么时间停药?最佳的免疫治疗时长如何确定?
目前,已开展的三期临床研究中对于治疗时长的规定,部分研究允许患者可持续治疗至疾病进展(PD),另也有部分研究规定患者可持续治疗至最长2年或出现不可接受的毒副反应。KEYNOTE-189和KEYNOTE-407研究中对于已完成研究规定的2年免疫治疗的患者进行了分析,在两项研究中,分别有57和55例患者完成了35个周期(2年)帕博利珠单抗治疗,长期随访数据显示,这部分接受了2年免疫治疗患者的长生存获益显著,3年OS率达到70%左右,进而说明ICIs持续治疗为患者带来持续获益。同时安全性数据显示,完成了35个周期免疫治疗的患者在更长的随访周期中,后续并未出现更多的irAE问题【3, 4】。然而,由于存在潜在的幸存者偏差,该数据为我们带来的提示作用还需进一步的探讨。
CheckMate 153研究进一步探索了免疫检查点抑制剂(ICIs)的用药时长与疗效及药物毒性之间的相关性【7】。该随机对照IIIB/IV期研究纳入了既往系统性化疗失败的晚期NSCLC患者,接受纳武利尤单抗治疗。后续将已完成1年纳武利尤单抗治疗的患者随机分为两组,继续接受纳武利尤单抗治疗(持续治疗组,N=127),或停用纳武利尤单抗(免疫治疗1年后停药组,N=125)。结果显示,与免疫治疗1年后停药的患者相比,持续治疗患者的PFS(24.7 vs 9.4个月,HR=0.56,95% CI: 0.37–0.84)和OS(NR vs 28.8个月,HR=0.62,95%CI: 0.42-0.92)均更长,其中PR/CR的患者能从后续持续治疗中获益更多(图1)。
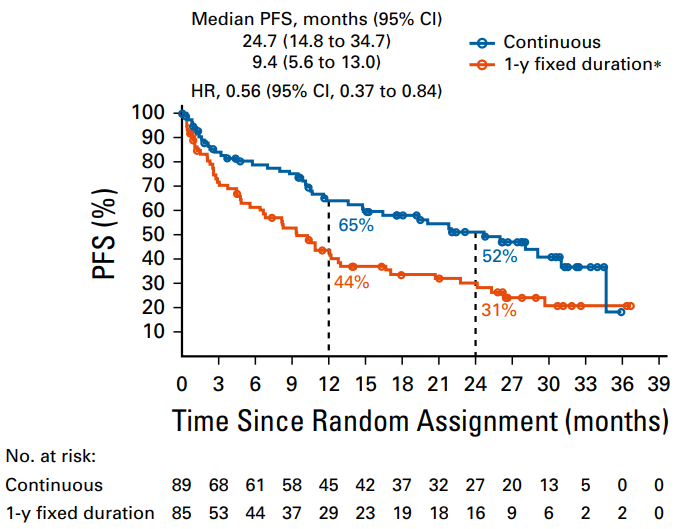
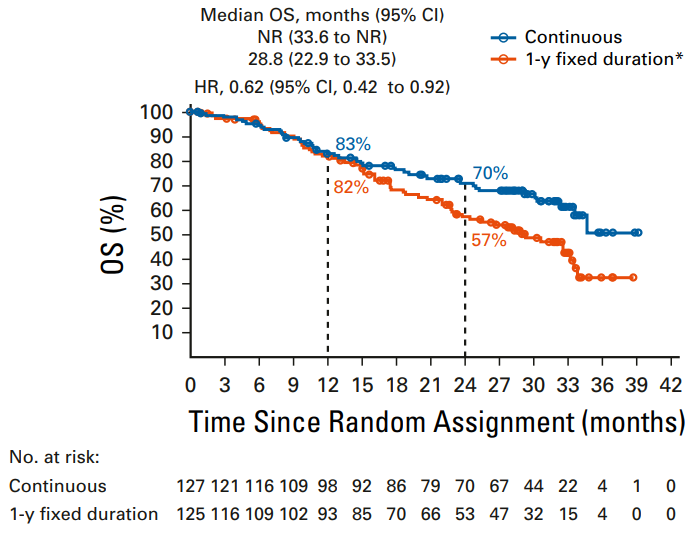
图1. CheckMate 153生存分析:超过1年免疫治疗 vs 1年免疫治疗【7】
RATIONALE 304是一项探索替雷利珠单抗联合化疗对比单纯化疗一线治疗晚期非鳞NSCLC的III期临床试验,该研究的探索性分析首次揭示了IO+化疗一线治疗晚期非鳞NSCLC的肿瘤缓解特征。结果显示,替雷利珠单抗联合化疗组应答者的中位至缓解时间(TTR)为7.9周(范围:5.1-33.3周),但患者首次获得缓解的时间存在较大个体化差异,近50%的应答者在第二次评估后(≥4周期治疗后)出现首次缓解。此外,在首次观察到肿瘤缓解后,75%的患者通过持续治疗肿瘤进一步退缩,从首次缓解到获得最大肿瘤缓解的中位时间为3.6个月(约5个周期),肿瘤缓解深度更深的应答者,PFS相对更长(图2)【6】,提示持续治疗可为患者带来持续获益,在条件允许的情况下,应尽可能防止治疗早期终止用药。
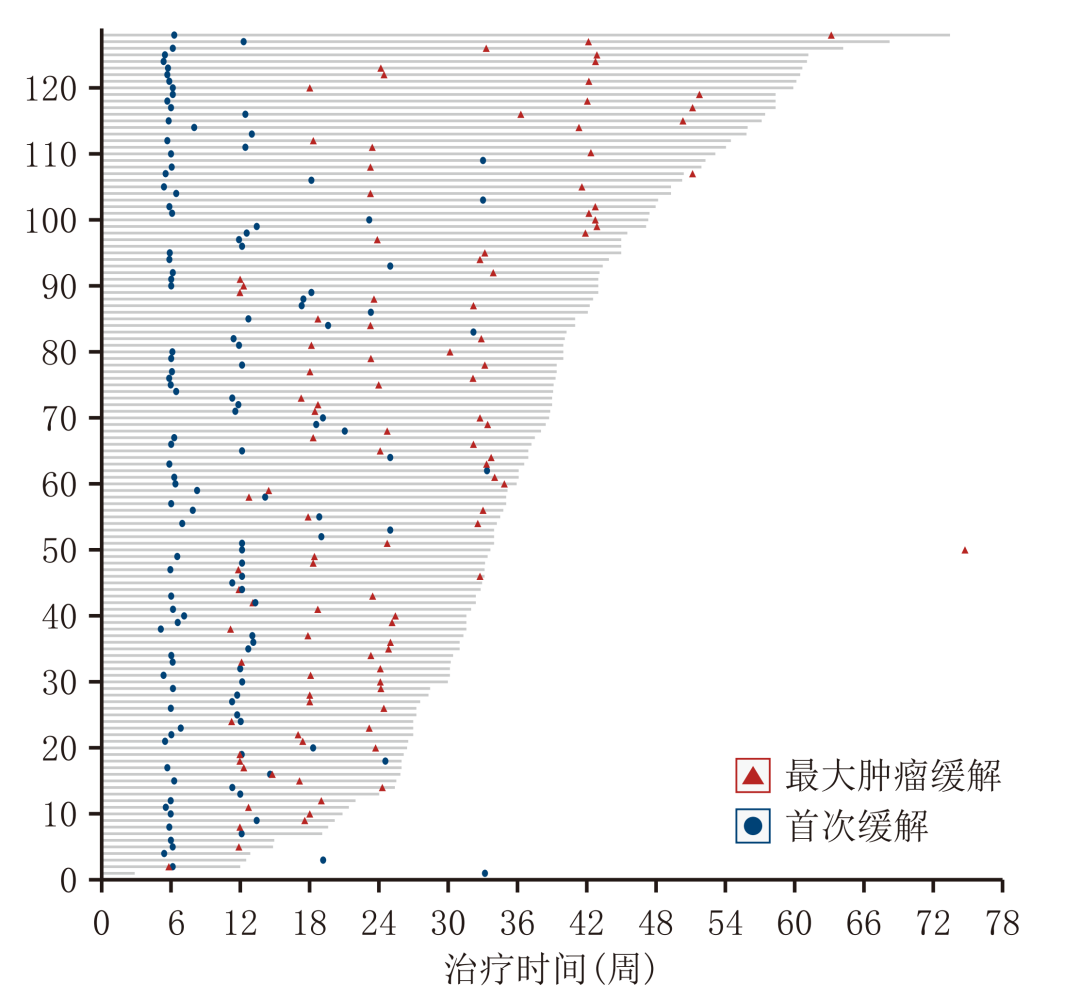
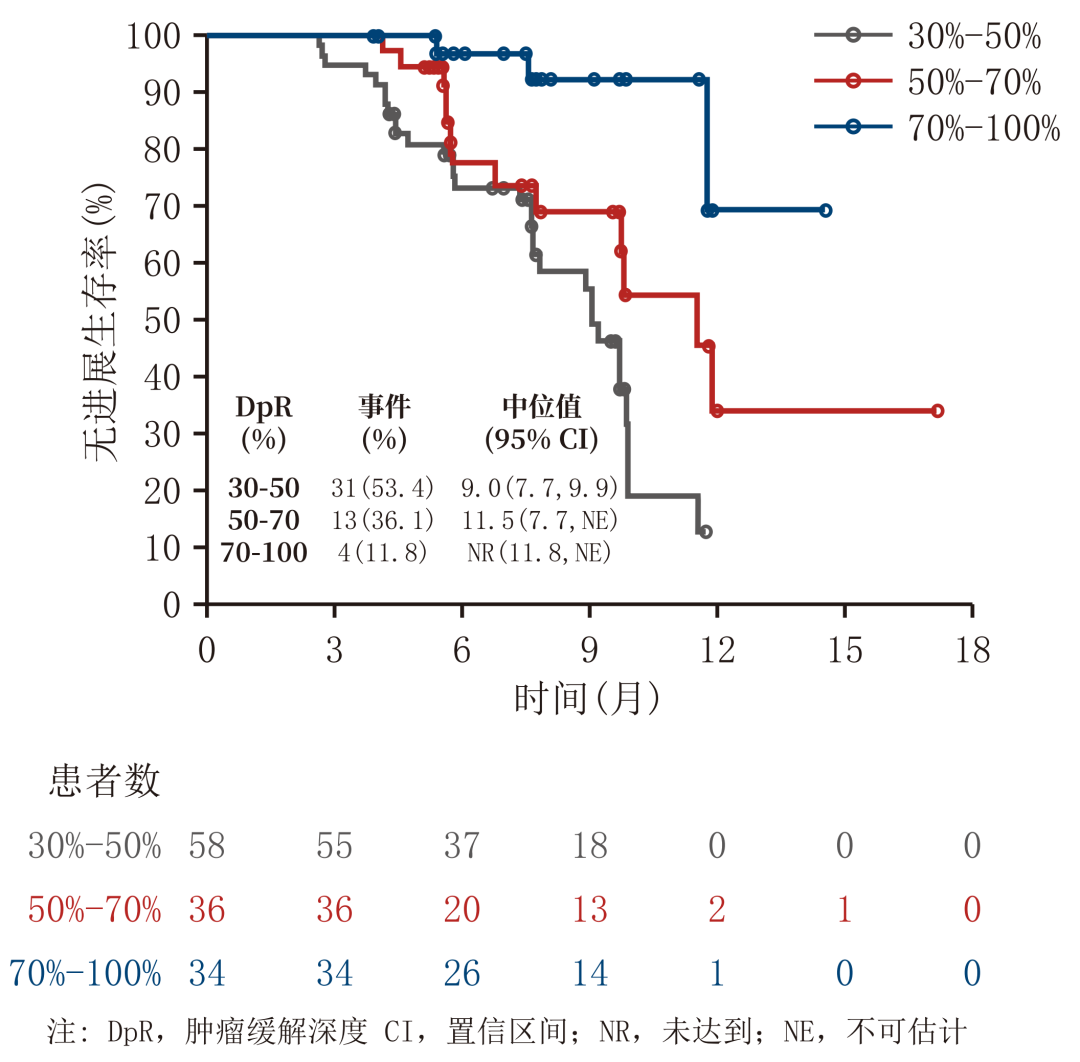
图2. 替雷利珠单抗联合化疗组应答者的肿瘤缓解情况及不同缓解深度应答者的PFS
【免疫进展后继续治疗(TBP)和免疫跨线治疗的探索】
免疫治疗已在晚期NSCLC的一线治疗中得到普及,然而尽管有部分患者能够取得长期生存获益,多数患者最终会面临免疫耐药,关于免疫治疗进展后的治疗策略选择,以及TBP或免疫跨线治疗的可行性,已成为了目前临床探索的热门话题。已有研究显示,针对特定人群,例如一线免疫治疗后出现局部进展的晚期NSCLC患者,继续原免疫治疗方案的同时联合局部治疗手段可能为患者带来获益,目前有多项相关研究正在探索之中【8】。而对于免疫治疗后广泛进展的晚期NSCLC患者,多项小样本研究提示,更换联合的化疗药物/抗血管等药物的免疫跨线方案,有望调节免疫微环境,逆转免疫耐药,潜在提升患者的后线治疗生存获益(图3)。
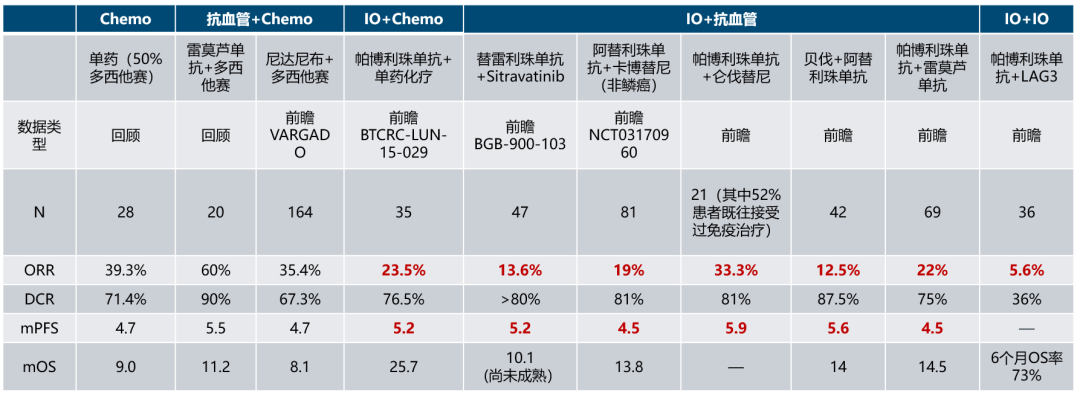
图3. 针对免疫耐药人群不同治疗策略的小样本研究探索
目前有多项III期临床研究正在开展免疫跨线治疗相关探索,期待相关研究结果能够为免疫耐药人群提供更多确证性的数据支持(图4)。
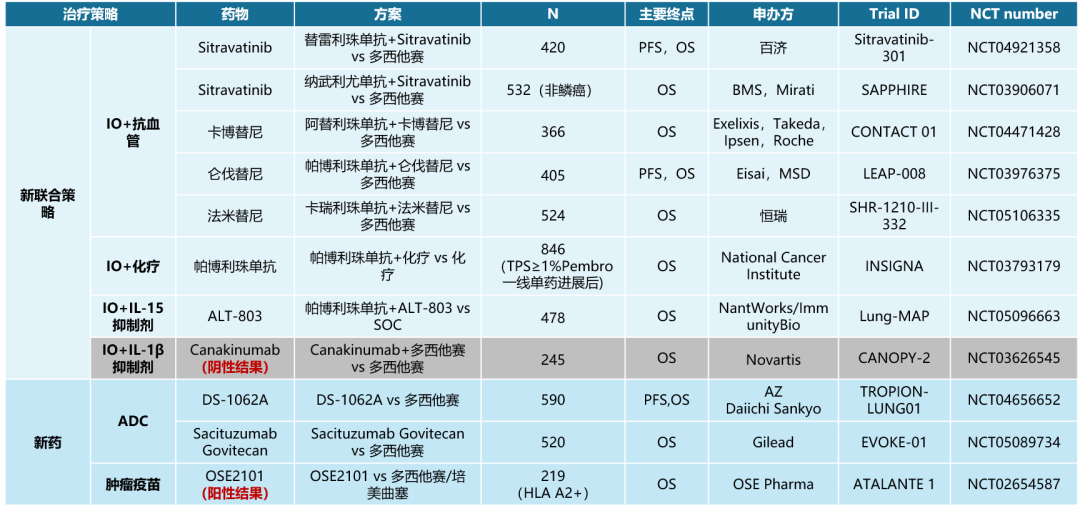
图4. 针对免疫耐药人群不同治疗策略的III期研究探索
【长期免疫治疗的药物毒性及经济负担】
如上文所述,研究数据表明晚期NSCLC患者的持续治疗以及免疫进展后继续治疗或跨线治疗方案可能为患者带来获益,但关于长期用药所带来的药物毒性风险以及患者所承受的经济负担也是现实中需要考虑的重要因素。免疫治疗相关不良反应通常发生在治疗的前5-15周,但现有的数据表明,在免疫治疗期间和停药后均会出现延迟发生的不良反应。相比于传统系统性治疗,免疫治疗所导致的不良反应率更低,但长期使用所带来的潜在毒性提升不容忽略。KEYNOTE-010试验的数据显示,毒性随着时间的推移而累积,每6个月约有10%的新患者发生≥3级不良事件【9】。在CheckMate 153研究中,如上文所述,与免疫治疗1年后停药的患者相比,持续治疗患者能够取得显著的生存获益提升,同时治疗相关不良事件发生率(48.0% vs. 26.4%)以及因不良事件导致治疗终止发生率(9.4% vs. 1.6%)也稍有提高,但无其它新发不良事件报道【6】。在经济负担方面,一项基于EMPOWER-LUNG1研究的分析显示,对于PD-L1高表达患者,与一线接受传统化疗相比,接受免疫治疗的总体经济成本更低【10】。另一项研究数据显示,当根据以OS表示的疗效来比较药物治疗的成本时,与传统治疗相比,免疫治疗在晚期NSCLC患者的一线和二线治疗中均显示出更低的经济成本。除此之外,目前已批准的免疫检查点类药物治疗均采用固定剂量输注,如果考虑患者的长期或终身治疗,与固定剂量相比,基于患者体重的治疗方案可能减少大约25-40%的额外药物剂量和25%的药物成本,进一步减轻患者的经济负担。
参考文献
【1】Putzu, Carlo et al. “Duration of Immunotherapy in Non-Small Cell Lung Cancer Survivors: A Lifelong Commitment?.” Cancers vol. 15,3 689. 22 Jan. 2023, 【2】Chen, Peixin et al. “Non-small cell lung cancer in China.” Cancer communications (London, England) vol. 42,10 (2022): 937-970.
【3】Novello, Silvia et al. “Pembrolizumab Plus Chemotherapy in Squamous Non-Small-Cell Lung Cancer: 5-Year Update of the Phase III KEYNOTE-407 Study.” Journal of clinical oncology : official journal of the American Society of Clinical Oncology, JCO2201990. 3 Feb. 2023.
【4】Garassino, Marina C et al. “Pembrolizumab Plus Pemetrexed and Platinum in Nonsquamous Non-Small-Cell Lung Cancer: 5-Year Outcomes From the Phase 3 KEYNOTE-189 Study.” Journal of clinical oncology : official journal of the American Society of Clinical Oncology, JCO2201989. 21 Feb. 2023.
【5】Zhou, Caicun et al. “Tislelizumab Versus Docetaxel in Patients With Previously Treated Advanced NSCLC (RATIONALE-303): A Phase 3, Open-Label, Randomized Controlled Trial.” Journal of thoracic oncology : official publication of the International Association for the Study of Lung Cancer vol. 18,1 (2023): 93-105.
【6】Waterhouse, David M et al. “Continuous Versus 1-Year Fixed-Duration Nivolumab in Previously Treated Advanced Non-Small-Cell Lung Cancer: CheckMate 153.” Journal of clinical oncology : official journal of the American Society of Clinical Oncology vol. 38,33 (2020): 3863-3873. doi:10.1200/JCO.20.00131
【7】Bayle, Arnaud et al. “Switch to anti-programmed cell death protein 1 (anti-PD-1) fixed-dose regimen: What is the economic impact?.” European journal of cancer (Oxford, England : 1990) vol. 113 (2019): 28-31.
【8】Prelaj, Arsela et al. “Beyond First-Line Immunotherapy: Potential Therapeutic Strategies based on Different Pattern Progressions: Oligo and Systemic Progression.” Cancers vol. 13,6 1300. 15 Mar. 2021, doi:10.3390/cancers13061300
【9】Akamatsu, Hiroaki et al. “Immune-Related Adverse Events by Immune Checkpoint Inhibitors Significantly Predict Durable Efficacy Even in Responders with Advanced Non-Small Cell Lung Cancer.” The oncologist vol. 25,4 (2020): e679-e683.
【10】Zhang, M et al. “First-line Cemiplimab versus Standard Chemotherapy in Advanced Non-small Cell Lung Cancer Patients with at Least 50% Programmed Cell Death Receptor Ligand-1 Positivity: Analysis of Cost-effectiveness.” Clinical oncology (Royal College of Radiologists (Great Britain)) vol. 34,3 (2022): e123-e129.
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。





