一、引言
肾脏,这个人体必不可少的器官,执行着清除代谢废物和过量水分的功能,同时也调节血压、电解质平衡和红细胞生成。当肾脏的结构或功能受到威胁时,如在局部肾切除术(PN)这种治疗肾脏肿瘤的手术中,它的功能可能会受到严重影响,导致急性肾损伤(AKI)。AKI不仅增加了患者的短期病死率,还可能导致长期健康问题。因此,了解和预测PN术后AKI的风险因素变得至关重要。
最近的一项研究[1],聚焦于这一领域,提供了关于术后AKI风险因素的新见解,特别是局部肾切除术中的缺血时间如何影响术后肾脏健康的风险。本文将深入探讨该研究的发现,并讨论其对肾脏疾病治疗和管理的潜在影响。
二、研究背景与目的
该研究之所以显得尤为重要,是因为局部肾切除术作为保留肾脏功能的首选治疗方式,在临床实践中广泛应用于早期肾脏肿瘤患者。然而,PN术中不可避免地会出现一段时间的肾脏缺血,即肾脏血液供应的暂时中断。虽然这一过程对于减少术中出血和提高肿瘤切除的准确性至关重要,但缺血时间的长短却与术后AKI的风险密切相关。AKI作为一个可能导致慢性肾病甚至终末期肾病的危险因素,其在术后的早期识别和预防变得至关重要。
为了深入探究这一现象,研究者们设计了一项前瞻性多中心研究,旨在评估PN术中缺血时间与AKI之间的关系,并尝试确定哪些患者更可能在手术后发展AKI。通过这项研究,医生们希望能够更好地预测和管理术后AKI,从而改善患者的治疗结果。
三、研究设计与方法
该研究收集了944名接受PN治疗cT1肾脏肿瘤的患者的数据,并对他们进行了长期的跟踪。研究者特别关注术后出现AKI的235名患者,并对比了有无AKI的患者的多种临床参数。其中最引人注目的是肾脏的缺血时间,以及这一变量如何与患者的基线特征和手术细节相互作用,最终影响AKI的发生率。
研究者利用分类与回归树(CART)分析对患者的AKI风险进行了分层,将患者分为高风险和低风险两组。这种方法的优势在于它能够考虑多个风险因素的交互作用,并提供一个个性化的风险评估。
四、研究结果的深入解读与分析
1、肾部分切术后有无AKI分组患者临床特征基线情况
图1表格列出了接受夹持型局部肾切除术治疗T1肾脏肿瘤的944名患者的描述性特征,并将他们根据术后是否出现AKI分为两组。具体分析如下:
- 年龄:平均年龄在AKI组稍高,这表明年龄可能与AKI风险有关。
- BMI(体质指数):两组的BMI中位数相似。
- 性别:AKI组中男性比例较高(71% vs. 61%),这可能表明男性在这项手术后更容易发展成AKI。
- 基线肾小球滤过率(eGFR):两组的eGFR中位数接近,表明术前肾功能不是AKI发生的显著预测因子。
- 高血压和糖尿病:这两个组中高血压和糖尿病的比例相近,表明这些条件可能不是AKI发生的关键影响因素。
- Charlson Comorbidity Index:较高的共病指数在AKI组更常见,尽管统计上未达到显著差异(p = 0.068)。
- ECOG评分:评估患者日常活动能力的ECOG评分在两组间没有显著差异。
- ASA评分:美国麻醉师学会(ASA)评分显示,两组患者的手术风险类似。
- 肿瘤侧别:肿瘤侧别(左侧或右侧)在两组间没有显著差异。
- 临床T阶段:T1b阶段的肿瘤在AKI组更常见,这可能表明肿瘤阶段与AKI风险有关。
- PADUA评分:一个评估肿瘤解剖位置及复杂性的评分,显示高PADUA评分与AKI风险显著相关。
- 手术方式:开放手术在AKI组中更常见,这可能表明手术方式是AKI风险的一个影响因素。
缺血时间:AKI组的缺血时间中位数显著长于无AKI组,这强烈表明缺血时间与AKI风险增加有关。
总的来说,这张表格展示的数据表明,年龄、性别、肿瘤阶段、PADUA评分、手术方式和缺血时间是与AKI风险增加相关的因素。这些因素的识别对于评估患者术后AKI风险、优化手术方案和提高患者护理质量至关重要。
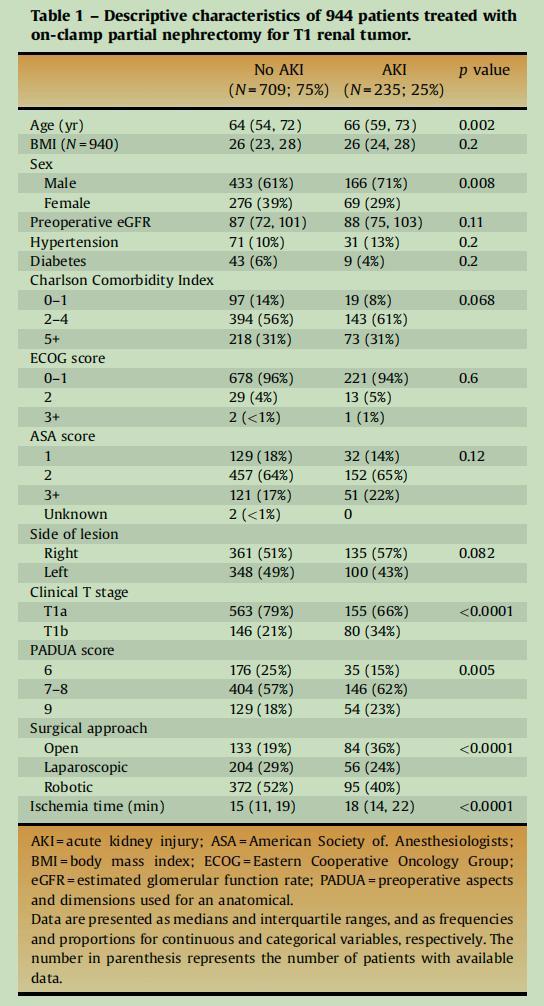
图1
2、肾部分切术后诱发AKI的相关因素
图2表格展示了在920名接受T1肾脏肿瘤部分肾切除术患者中,多变量逻辑回归分析用于预测术后AKI的结果。以下是对该表格的解读:
- 年龄:Odds ratio(OR)为1.03,95%置信区间(CI)为1.02至1.05,p值<0.0001。这意味着年龄的每增加一年,AKI的风险平均增加3%。年龄是一个显著的风险因素。
- 临床T阶段:T1b相比T1a(参考组),OR为1.88,95% CI为1.35至2.62,p值为0.0002。这表明T1b阶段的肿瘤比T1a阶段的风险高88%。
- PADUA评分:PADUA评分每增加一点,AKI的风险增加20%,OR为1.20,95% CI为1.05至1.37,p值为0.007。PADUA评分是评估肿瘤解剖特点和手术难度的一个工具,这个结果表明评分越高,AKI风险越大。
- 术前肾小球滤过率(eGFR):术前估算肾小球滤过率(eGFR)越高,AKI的风险越高,OR为1.02,95% CI为1.01至1.03,p值为0.003。这意味着肾功能越好,AKI的风险略微增加。这似乎是一个非直观的结果,可能的原因是:如果患者术前肾功能很好,那么相对的肾功能下降(即使是绝对数值不大)可能更容易达到AKI的诊断标准。例如,一个健康的肾脏可能会在肾脏被损伤时表现出相对较大的肌酐水平变化,而那些已经有损伤的肾脏则不会表现出这样显著的变化。
- 手术方式:与开放手术相比,腹腔镜手术的OR为0.47,95% CI为0.26至0.84,p值为0.011;机器人辅助手术的OR为0.39,95% CI为0.25至0.60,p值<0.0001。这表示与开放手术相比,腹腔镜手术和机器人辅助手术分别降低了53%和61%的AKI风险。腹腔镜手术和机器人辅助手术与开放手术相比,显著降低了AKI的风险。这一结果可能由以下几个因素导致:①较小的切口和更精细的操作可能导致的组织损伤更少;②减少组织创伤能够减轻炎症反应,从而可能减少术后肾脏的应激。③缺血时间的缩短:使用机器人辅助和腹腔镜手术可能缩短了肾脏的缺血时间。技术先进的设备和精准的操控可以使得手术过程更加迅速和精确,从而缩短血流阻断的时间。④出血量的减少:这些手术方法可能与更少的出血量相关,因此减少了术后肾功能不全的风险。
综上所述,这些统计数据显著地指出了与术后AKI风险增加相关的多个因素,包括年龄、肿瘤阶段、PADUA评分和术前肾功能。此外,手术方式也是一个重要因素,其中腹腔镜和机器人辅助手术似乎比开放手术有更低的AKI风险。这些发现可以帮助医生在术前评估AKI的风险,并在可能的情况下选择更低风险的手术方法。
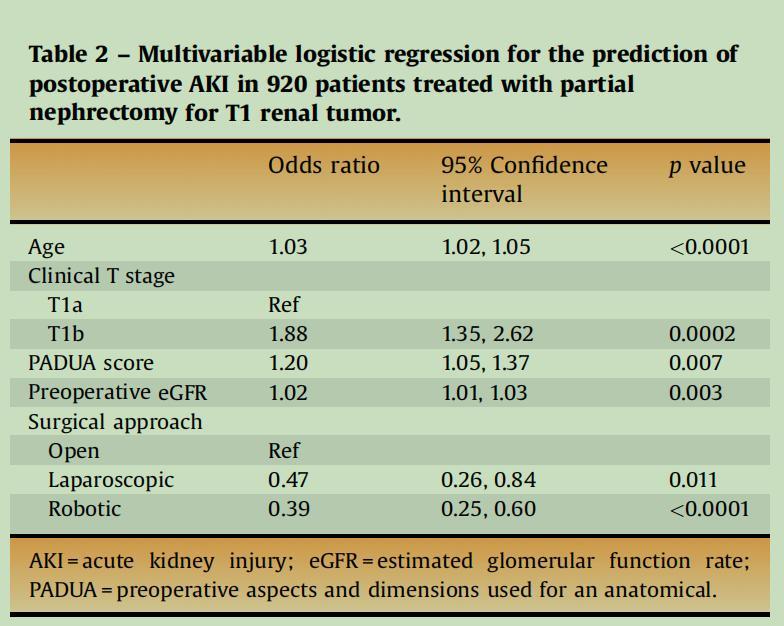
图2
3、根据术前AKI风险分层,AKI与缺血时间之间的关系
图3展示的是术中缺血时间与术后AKI发生率之间的关系,并根据术前AKI风险进行了分层。具体解读如下:
- 红线:代表术前AKI风险大于40%的患者群体。这条线显示了随着缺血时间的增加,观察到的AKI发生率明显升高。特别是在缺血时间超过大约25分钟后,AKI的概率急剧上升,接近100%。
- 虚线:代表术前AKI风险小于或等于40%的患者群体。对于这个群体,缺血时间与AKI发生率的关系相对平缓。即使在缺血时间超过25分钟时,AKI的发生率也远低于高风险患者群体。
总的来说,对于高风险患者,缺血时间对AKI的影响更大。这意味着在考虑延长缺血时间时,术前评估AKI风险是非常重要的。似乎存在某个缺血时间的阈值,在这个点后AKI风险增加显著。对于高风险患者,这个阈值可能在20分钟左右,而对于低风险患者可能会更长。图中数据强调了个体化医疗的重要性,即在手术前进行风险评估可以帮助预测术后AKI的风险,并指导手术决策。例如,对于术前被评估为高风险的患者,可能需要采取更加激进的风险管理策略,比如选择使用更先进的手术技术,或实施额外的肾脏保护措施。
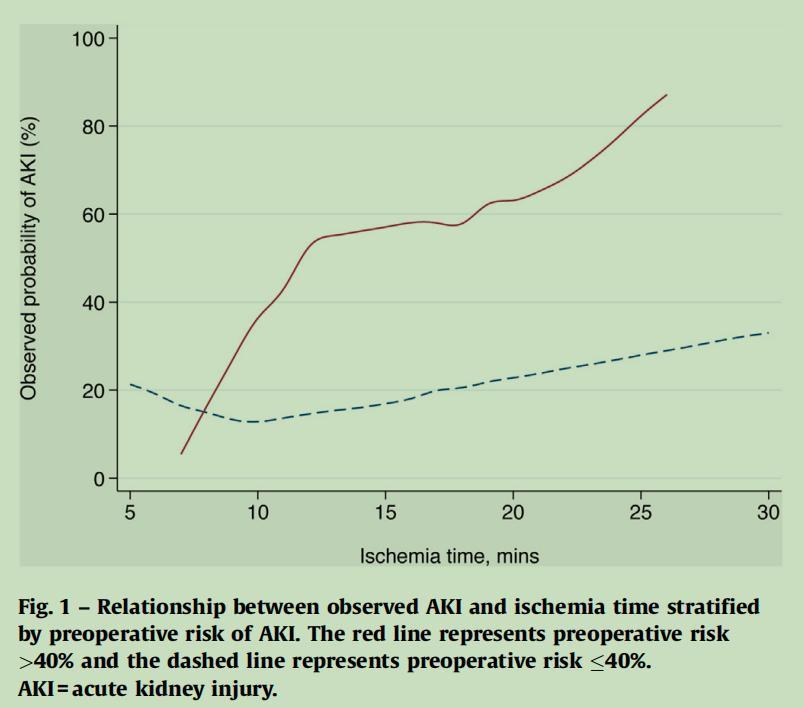
图3
五、该研究的临床应用价值
该研究为泌尿外科医生提供了重要的实证依据,有助于提高肾部分切除术的安全性和效果,减少AKI的风险,并为患者提供更加个性化和优化的治疗方案。
1、术前风险评估:通过识别与术后AKI风险相关的因素,如年龄、肿瘤特征(T阶段和PADUA评分)、术前肾小球滤过率(eGFR),以及手术方式,该研究提供了一个更全面的术前评估框架。医生可以利用这些信息来评估患者进行局部肾切除术的AKI风险,并据此制定个性化的治疗计划,可能包括选择最佳的手术方式和准备相应的肾脏保护措施。
2、手术策略优化:研究发现,与开放手术相比,腹腔镜和机器人辅助手术有更低的AKI风险。这一发现支持微创手术在适当的患者中的应用,并可能鼓励更广泛地采用这些技术,以减少术后并发症。
3、缺血时间管理:研究明确指出了缺血时间与AKI风险之间的关系,并揭示了缺血时间在高风险患者中对AKI的影响更为显著。这强调了术中缺血时间管理的重要性,特别是在被评估为高AKI风险的患者中。
4、个体化治疗:通过CART分析对患者进行高风险和低风险分层,该研究为个体化治疗提供了科学依据。不同风险水平的患者可能需要不同的监测和管理策略,以最小化术后AKI的风险。
5、术后监测和管理:该研究还提示了术后监测的重要性,对于高风险患者,密切监测其肾功能的变化,及时发现和处理AKI,可能有助于改善长期肾脏健康和整体预后。
六、结论
本研究深入探讨了局部肾切除术中缺血时间与术后AKI之间的关系。研究发现,年龄、肿瘤特征、术前估算肾小球滤过率(eGFR),以及手术方式均与AKI风险显著相关,且微创手术方式在减少AKI风险方面表现出明显优势。这些发现对于指导临床实践、改善患者预后、并推动个性化治疗计划的制定具有重要价值。
尽管如此,该研究也存在一些局限性。首先,其回顾性设计可能导致了患者选择偏差和信息偏差。其次,由于研究采用的是多中心数据,不同中心之间的手术技术和术后管理的差异可能会影响结果的一致性。此外,研究没有详细考虑患者术前共病情况和生活习惯等潜在影响因素,这些因素可能会对AKI风险产生影响。最后,缺乏长期随访数据限制了我们对术后AKI对慢性肾病和长期生存影响的理解。
未来的研究应该着重于克服这些局限性,例如,进行更为细致的前瞻性队列研究以验证和细化这些初步发现。同时,未来研究应当更全面地收集数据,以包括患者的生活方式、营养状况和遗传背景等变量。进一步的研究还应当探索不同肾脏保护策略的有效性,以及这些策略如何在不同风险群体中的应用。此外,长期随访研究对于评估AKI对患者长期健康影响至关重要,这有助于我们更好地理解和改善肾部分切除术的长期治疗效果。通过这些努力,我们可以期待未来会有更多针对性的预防措施和治疗策略的出现,以优化患者的术后恢复和长期肾功能。
参考文献:
[1] Bravi CA, Mari A, Larcher A, Amparore D, Antonelli A, Artibani W, Bertini R, Bove P, Brunocilla E, Da Pozzo L, di Maida F, Fiori C, Gallioli A, Gontero P, Li Marzi V, Longo N, Mirone V, Porpiglia F, Rocco B, Schiavina R, Schips L, Simeone C, Siracusano S, Tellini R, Terrone C, Trombetta C, Ficarra V, Carini M, Montorsi F, Capitanio U, Minervini A. Toward Individualized Approaches to Partial Nephrectomy: Assessing the Correlation Between Ischemia Time and Patient Health Status (RECORD2 Project). Eur Urol Oncol. 2021 Aug;4(4):645-650. doi: 10.1016/j.euo.2020.05.009. Epub 2020 Jul 6. PMID: 32646849.
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。





