导读HIV检测的初筛结果如果为阳性,按照规范的检测流程,将进入到HIV的补充试验,做进一步的检测。
HIV检测的初筛结果如果为阳性,按照规范的检测流程,将进入到HIV的补充试验,做进一步的检测。下面就艾滋病的主要的补充试验,做一个浅显的介绍。
一、何谓补充试验
在《全国艾滋病检测技术规范》(2009版)中,如筛查结果为阳性的样本,将进行下一步的确证试验,而在2015版中,国家将核酸试验以及特定条件下的替代检测,和确证试验一起作为补充试验,其检测结果都是可以作为判定是否感染艾滋病病毒的重要依据。
补充试验是通过检测样本中是否存在艾滋病病毒抗体、抗原或者核酸而确定艾滋病病毒感染的检测方法。
补充试验一般指:抗体确证试验,核酸试验,在特定条件下的替代检测。
抗体确证试验包括免疫印迹试验,条带/线性免疫试验,这个是在日常工作中最常使用的检测方法。
核酸试验主要是对一些特殊的人员使用这种方法,结合临床,来判断是否感染了艾滋病病毒。
替代检测包括三种酶联免疫试验、三种快速试验或酶联免疫加快速试验。
二、确证试验
目前在实际工作中常用的确证试验,包括免疫印迹试验(WB),条带/线性免疫试验(RIBA/LIA)。
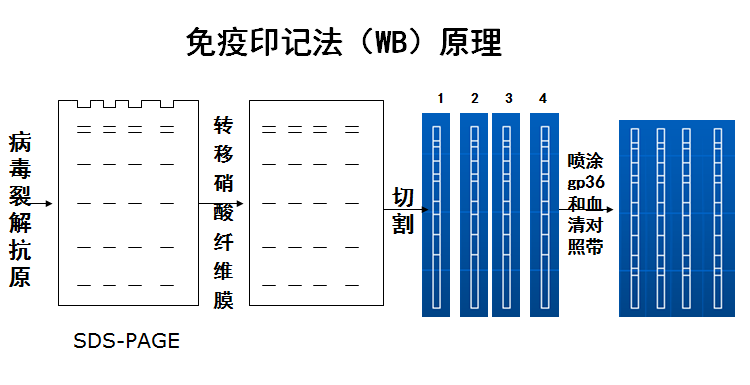
1、免疫印迹试验WesternBlot(WB):
WB采用间接法检测样品中的抗HIV-1/HIV-2特异性抗体。采用聚丙烯酰胺凝胶电泳把分子量大小不等的HIV-1蛋白分离开来,然后再把这些分离的不同蛋白带转移到硝酸纤维素膜上(或PVDF膜)。将此膜切割成条状,每一膜条上均含有经电泳分离过的HIV抗原。待测样品经适当稀释后,加至硝酸纤维素膜上,恒温震荡,使其充分接触反应,血清中若含有HIV抗体,就会与膜条上抗原带相结合。加入抗人-IgG酶结合物和底物后,根据出现条带情况,按照试剂盒说明书判定标准,判断待测样品为阳性、阴性或不确定。
WB是目前特异性、敏感性均比较好的证实HIV感染的方法。也是国内HIV确认的首选方法,它是在DNA印迹术的基础上发展而来的新型技术。据报道,WB试验有2%的假阳性,多见于伴有自身免疫性疾病或打过疫苗的患者。如果将EIA和WB结合起来进行HIV特异性抗体检测,可以将检测结果的准确率提高至99%,假阳性率0.0006%。
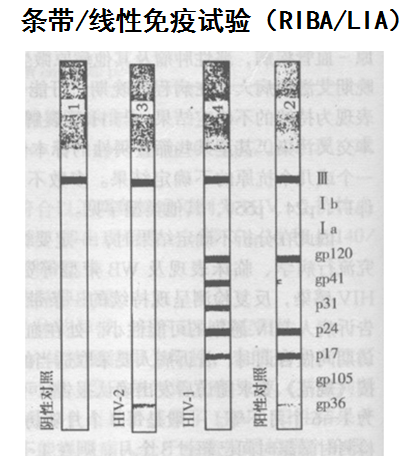
2、条带/线性免疫试验(RIBA/LIA)
RIBA/LIA采用间接法检测样品中的抗HIV-1/HIV-2特异性抗体,试剂盒的膜条上包被有HIV-1/HIV-2不同的重组抗原片段,加入待测样品后,其中的相应抗体与抗原发生特异性的免疫反应;随后加入抗人IgG(碱性磷酸酶标记)与HIV特异性IgG抗体相结合;加入显色底物后,在碱性磷酸酶的催化下,特异性抗体的结合部位出现肉眼可见的条带,按照试剂盒说明书判定标准,判断待测样品为阳性、阴性或不确定。

这个方法的原理和WB和相同的,只是由于膜条包被的是基因工程表达的或合成肽HIV重组抗原片段,不像是WB上的自然的灭活全病毒抗原,由于人工重组后,抗原的纯度较高,减少了一些干扰物质,所以特异性较好,不确定结果相对减少30%~60%,但同时由于只是选取了一些相对比较特异的条带,而不是全病毒的所有条带,所以敏感性相对要低一些,假阴性要高一些。
3、结果判断
确认方法的结果是要根据不同厂家的说明书来做判断的,看出现不同的条带来做判断,其中HIV-1抗体特异带包括:env带:gp160/gp120、gp41;gag带:p55、p24、p17(或p18);pol带:p66(或p65)、p51、p31。HIV-2抗体特异条带包括:env带:gp140/gp105、gp36;gag带:p56、p26、p16;pol带:p68、p53、p34。(由于使用的毒株不同,HIV-2env带也可为gp125/gp80、gp36)。
一般是需要同时符合以下2条标准可判为HIV-1抗体阳性:①至少有2条env带(gp41和gp160/gp120)出现,或至少1条env带和p24带同时出现;②符合试剂盒提供的阳性判定标准。对于出现HIV-2型特异性指示带的样品:如果同时呈HIV-1抗体阳性反应,报告HIV-1抗体阳性,不推荐进一步做HIV-2抗体确证试验;如果同时呈HIV-1抗体不确定或阴性反应,需用HIV-2型确证试剂再做HIV-2的抗体确证试验。
出现HIV抗体特异带,但不足以判定阳性,结果为不确定。
无HIV抗体特异带出现,结果可判为阴性。
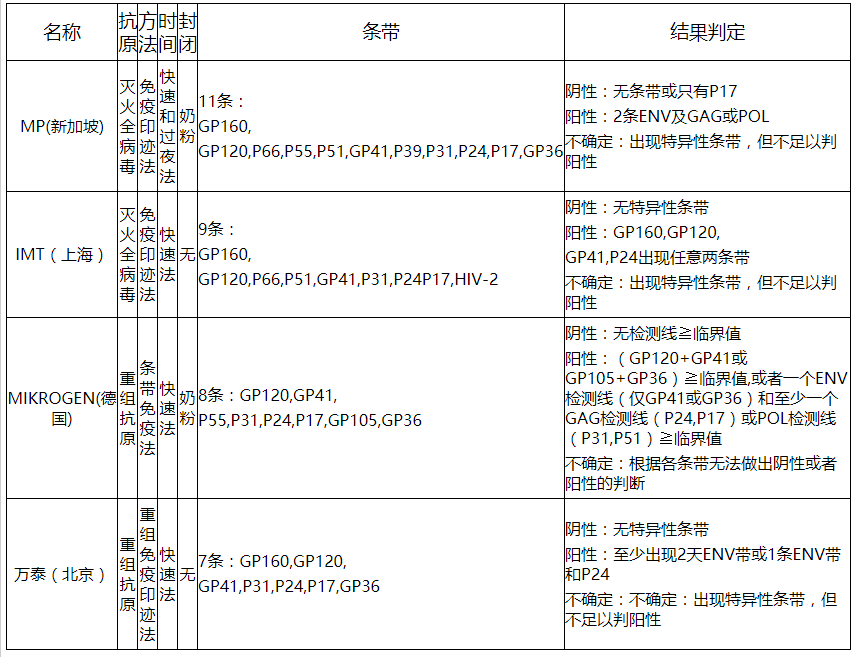
以下为几种常见试剂盒的结果判断:

三、核酸试验
核酸检测是对感染者体内游离病毒的核酸RNA含量进行测定。通常使用血浆作为检测样品,根据不同检测要求改进的RNA提取技术使该实验也可用于多种体液及组织。
核酸检测作为补充实验可用于HIV-1感染诊断,包括抗体复检试验有反应和抗体补充试验不确定样本的判定;急性期和晚期感染者的诊断。
针对对HIV-1抗体筛查阴性、近期有流行病学史的个体,或确证结果不确定的样本,核酸检测可用于诊断HIV-1急性期感染。
针对HIV-1抗体筛查阳性或确证结果不确定的个体,结合流行病学史和临床病史,核酸检测可用于HIV-1感染诊断。艾滋病晚期患者可能出现HIV抗体反应不确定,可根据HIV核酸检测结果,结合临床病史和CD4+T淋巴细胞计数等情况,进行综合判断,确定临床诊断。
但核酸检测结果低于最低检测限并不能完全排除HIV-1感染。
1、核酸定性试验:
全球目前正式用于临床诊断HIV-1急性期感染的核酸检测试剂比较少,主要是美国FDA批准的Gen-Probe公司生产的AptimaHIV-1RNA核酸定性检测试剂和欧盟批准的AbbottM2000HIV-1RNA/DNA定性检测试剂。国内生产的用于血浆及其血液制品筛查的核酸检测试剂主要为Taqman实时荧光PCR检测试剂。
检测结果显示“有反应”或“检测到”,报告阳性;检测结果显示“无反应”或“未检测到”,报告阴性。核酸定性检测值低于最低检测限的结果,不能排除HIV-1感染,需根据流行病学史、临床病史和实验室相关指标进行综合判断。
2、核酸定量试验:
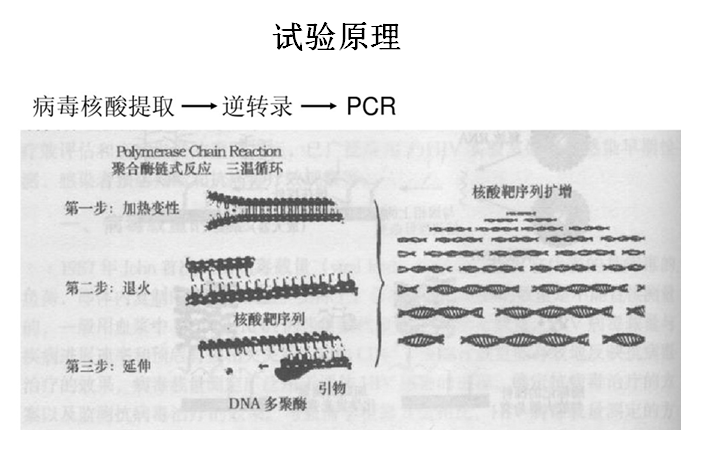
核酸定量检测原理主要基于靶核酸扩增RT-PCR和信号放大扩增,目前使用的病毒载量检测技术主要有三种:1、逆转录多聚酶链反应系统(RT-PCR)2、分支DNA信号扩大系统(bDNA)3、核酸序列扩增系统(NASBA),三种技术都有核酸提取、扩增或信号放大、定量检测三部分组成。

定量的核酸检测可以作为HIV-1感染的确认,但更多的是作用是监测抗病毒药物治疗效果和监测疾病进展。
核酸定量检测过程中,由于可能会受到的污染,从而导致低病毒检测值的结果,所以一般是以5000CPs/ml作为判断结果的阈值,检测值>5000CPs/ml(或IUs/ml),报告检测值;检测值≤5000CPs/ml(或IUs/ml),需再次采样检测,报告检测值,结果>5000CPs/ml(或IUs/ml),报告检测值,结果仍≤5000CPs/ml,则需充分结合流行病学史、临床病史、CD4+T淋巴细胞计数和HIV-1抗体随访检测结果等进行综合判断。
目前国内外均没有商品化的HIV-2核酸检测试剂。
四、替代检测:
替代检测一般在一些特定条件下使用这种检测策略,例如高流行地区(流行率大于5%)、高危人群(如男***性恋,***人群),就是用三种酶联免疫、三种快速试验或酶联加快速试验,进行检测,这个三种试剂均要经过使用地区中心实验室的评价。这个一般适用于某些特定的专项调查工作,在日常的工作中基本不使用这种方法。
五、补充试验的检测流程:
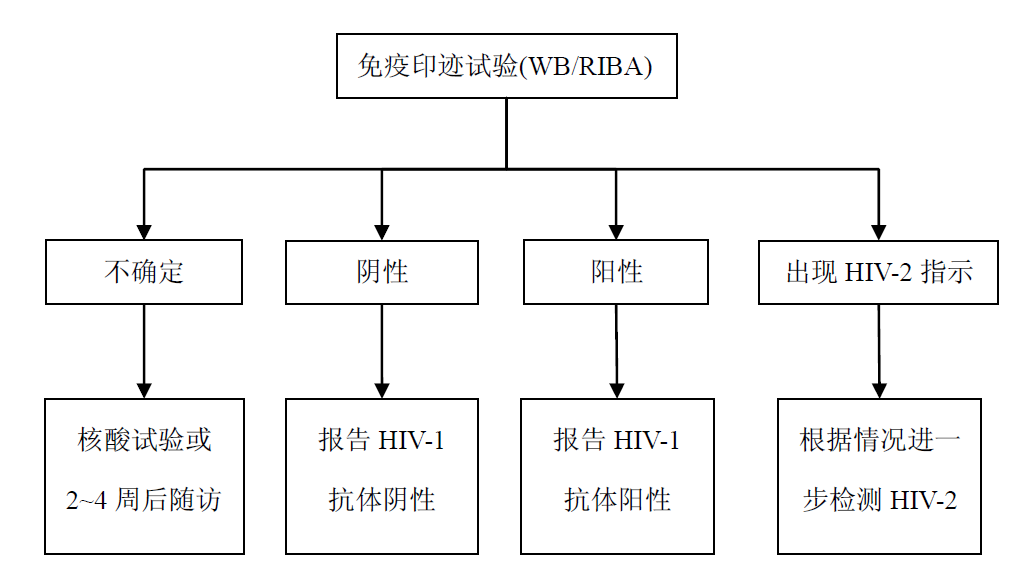
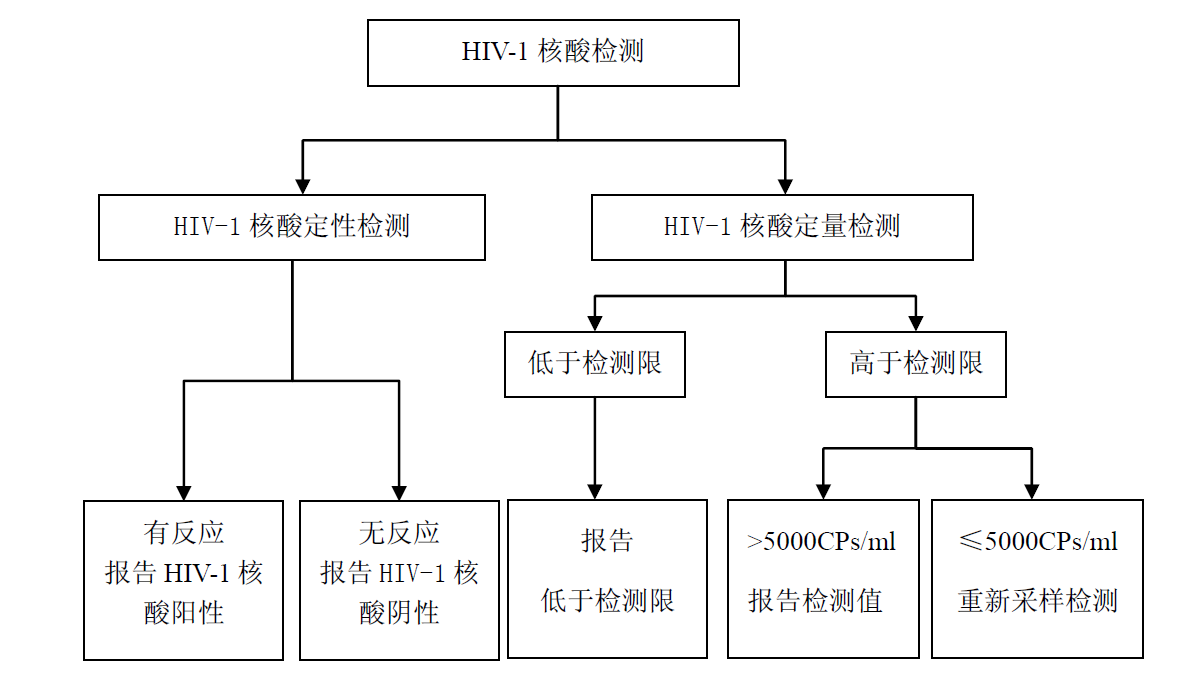
版权声明:
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。
本站所注明来源为"爱爱医"的文章,版权归作者与本站共同所有,非经授权不得转载。
本站所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,如果您认为我们的转载侵犯了您的权益,请及时通过电话(400-626-9910)或邮箱(zlzs@120.net)通知我们,我们将第一时间处理,感谢。





